Le zinc est utilisé depuis des millénaires sous forme d’alliage ou de minerai. Des objets en laiton, alliage de zinc et cuivre, ont été retrouvés et datés du 3ème millénaire avant notre ère. Malgré cette utilisation ancienne, le nom zinc, de l’allemand zinke pointe acérée, n’a été donné qu’au XVIème siècle par Paracelsus en référence à la forme du métal après fusion.
Données physico-chimiques
Données atomiques
| Numéro atomique | Masse atomique | Configuration électronique | Structure cristalline | Rayon métallique pour la coordinence 12 |
| 30 | 65,38 g.mol-1 | [Ar] 3d10 4s2 | hexagonale compacte de paramètres a = 0,2665 nm et c = 0,4947 nm | 139,4 pm |
Données physiques
| Masse volumique | Dureté | Température de fusion | Température d’ébullition | Conductibilité électrique | Conductibilité thermique | Solubilité dans l’eau |
| 7,14 g.cm-3 | 2,5 | 419,58°C | 907°C | 16,6.106 S.m-1 | 116 W.m-1.K-1 | insoluble |
Données chimiques
| Électronégativité de Pauling | pKa : Zn2+aq/ZnOH+aq | pKs : Zn(CN)2 | pKs : Zn(OH)2 | pKs : ZnS blende | pKs : ZnS wurtzite | pKs : Zn(IO3)2 |
| 1,65 | 9 | 22,6 | 16,1 | 23,7 | 21,5 | 5,4 |
Potentiels standards :
| Zn(OH)2 + 2e = Zn(s) + 2OH– | E° = -1,24 V |
| Zn(OH)42- + 2e = Zn(s) + 4OH– | E° = -1,21 V |
| Zn2+ + 2e = Zn(s) | E° = -0,76 V |
Données thermodynamiques
Zinc cristallisé :
|
Zinc gazeux :
|
Données industrielles
Matières premières
La teneur moyenne en zinc de l’écorce terrestre est de 80 ppm.
Les émissions atmosphériques naturelles de zinc liées au volcanisme, à l’érosion des roches… sont estimées à 5,9 millions de t/an. Les émissions liées aux activités humaines sont estimées à 57 000 t/an.
Dans les minerais, le zinc est très souvent associé à Pb et Cd ainsi qu’à Fe, Cu, Bi, Sb, As, Ge, In, Ag, Au…. Les minerais de zinc sont la principale source de cadmium, germanium et indium.
Minerais : le principal est la blende ou sphalérite (ZnS), les autres sont la smithsonite (ZnCO3), l’hémimorphite ou calamine (Zn4Si2O7(OH)2,H2O). La blende représente 95 % de la production minière.
La teneur des minerais tout venant est comprise entre 4 et 20 % de Zn. 80 % des exploitations minières représentant 64 % de la production sont souterraines, 8 % (15 % de la production) à ciel ouvert et 12 % (21 % de la production) associent les 2 types d’exploitation. En 2024, il y avait 333 mines de plomb et de zinc en exploitation dans le monde.
Principales mines en activité, d’après la production de 2025 :
| Rampura Agucha (Inde), en 2024-25 | 515 | Peñasquito (Mexique) | 231 | |
| Red Dog (États-Unis) | 463 | Dugald River (Australie) | 183 | |
| Antamina (Pérou) | 454 | San Cristóbal (Bolivie), estimation | 179 | |
| Mount Isa (Australie) | 288 | Gamsberg (Afrique du Sud), en 2024-25 | 133 | |
| Mc Arthur River (Australie) | 275 | Vazante (Brésil) | 128 |
- L’une des plus grande mine de zinc au monde, jusqu’en 2008 et entre 2015 et 2024, est celle de Red Dog, en Alaska. L’exploitation, à ciel ouvert, par Teck, a démarré en 1990, le gisement avait été découvert en 1968. Fin 2025, les réserves prouvées et probables sont de 22,8 millions de t de minerai contenant 11,2 % de Zn, 3,1 % de Pb et 57,4 g/t d’argent. En 2025, la production a été de 462 700 t de Zn, 107 000 t de Pb et 355 t d’argent. 30 % de la production de concentrés de zinc est traité dans la raffinerie exploitée par Teck, à Trail, au Canada, en Colombie Britannique. L’épuisement de la mine principale (Red Dog « Main ») est compensé par l’exploitation de gisements adjacents dont Red Dog « Aqqaluk » également à ciel ouvert. Les conditions climatiques ne permettent l’exportation des concentrés miniers que durant 100 jours entre les mois de juillet et octobre.
Aux États-Unis, la production avec 6 mines en exploitation provient, en 2024, à 81 % d’Alaska avec la mine de Red Dog (555 600 t de Zn) et celle de Greens Creek exploitée par Hecla Mining avec 51 200 t de Zn. - De 2008 à 2014, la plus importante mine de zinc dans le monde a été celle de Rampura Agucha, dans le Rajasthan, en Inde, exploitée par Hindustan Zinc, détenu à 64,9 % par Vedanta et 29,5 % par l’État indien. Sa production a été, en 2024-25, de 515 000 t de zinc et 52 000 t de plomb. Les réserves prouvées et probables sont de 46,8 millions de t de minerai renfermant 10,7 % de Zn, 1,1 % de Pb et 37 g/t de Ag. La mine a effectué une transition entre une exploitation à ciel ouvert et une exploitation souterraine.
- La mine de zinc d’Antamina, au Pérou, est détenue par Glencore à 33,75 %, BHP-Billiton à 33,75 %, Teck à 22,5 % et Mitsubishi à 10 %. Elle est située dans la cordillère des Andes entre 4 200 et 4 700 m d’altitude, dans la province de Huari. Le minerai, extrait à ciel ouvert, est concentré puis mis en suspension dans l’eau et envoyé à l’aide d’un minéralduc de 302 km de longueur jusqu’au port de Punta Lobitos situé près de Port Huarmey afin d’être exporté. Le minéralduc de 21 à 25 cm de diamètre est enfoui à 1 m de profondeur. Le trajet dure environ 50 h, avec une capacité de 2,5 millions de t/an. Les réserves prouvées et probables sont, fin 2025, de 528 millions de t avec 0,59 % de Zn, 0,91 % de Cu, 0,02 % de Mo et 12 g/t de Ag, ainsi que du plomb et du bismuth. En 2025, la production a été de 454 000 t de Zn, 381 800 t de Cu, 2 500 t de molybdène, 360,6 t d’argent, en 2023 et, en 2021, 7 407 t de plomb. La production a débuté en 2001.
- En Australie, exploitée par Glencore, la mine de Mc Arthur River a produit, en 2025, 274 600 t de Zn, 52 300 t de Pb et 64,7 t de Ag. Les réserves prouvées et probables sont, fin 2025, de 71 millions de t renfermant 8,85 % de Zn, 4,15 % de Pb et 42 g/t de Ag. Les mines de Mount Isa, regroupées avec celles de Lady Loretta et George Fisher, en Australie au nord-ouest de la province du Queensland, exploitées également par Glencore ont produit, en 2025, 288 200 t de zinc, 90 700 t de plomb et 116,5 t d’argent. Ce complexe minier produit également du cuivre, avec 54 100 t. Les réserves prouvées et probables sont, fin 2025, de 57 millions de t de minerai de zinc contenant 6,62 % de zinc, 3,55 % de plomb et 66 g/t d’argent.
- La mine de Peñasquito, au Mexique, est exploitée par le groupe Newmont. Elle a été acquise, début 2019, auprès de Goldcorp. C’est une mine d’or qui a produit, en 2025, 12,9 t d’or, 871 t d’argent, 231 000 t de zinc et 98 000 t de plomb. Fin 2025, les réserves prouvées et probables sont de 221 millions de t renfermant 0,67 % de Zn, 0,30 % de Pb, 32,4 g/t de Ag et 0,45 g/t de Au.
- En février 2019 a été inaugurée la mine de Gamsberg, en Afrique du Sud, développée par le groupe indien Vedanta, avec une production qui devrait atteindre 250 000 t/an de Zn. En 2024-25, la production a été de 133 000 t de Zn et 86 t de Pb, en 2023-24. Les réserves sont de 88,9 millions de t renfermant 6,0 % de Zn et 0,5 % de Pb.
- La mine à ciel ouvert de San Cristóbal, en Bolivie, était exploitée par le groupe japonais Sumitomo Corporation qui a vendu sa participation en 2023 à une société canadienne. En 2024, la production de concentrés de zinc-argent a été de 338 000 t et celle de concentrés de plomb-argent de 103 000 t. Les concentrés sont transportés par voie ferrée jusqu’au port de Mejillones, au Chili.
- En novembre 2017, la mine de Dugald River, dans la province du Queensland, en Australie, exploitée par MMG, détenu par le groupe chinois China Minmetals, est entrée en production. En 2025, la production a été de 183 463 t de Zn, 21 666 t de Pb et 48,8 t de Ag. Les réserves prouvées et probables, mi 2025, sont de 24 millions de t renfermant 10,7 % de Zn, 1,6 % de Pb et 28 g/t de Ag.
- Les mines de Cerro Lindo, au Pérou, et Vazante, au Brésil, sont exploitées par Nexa Resources, filiale du groupe brésilien Votorantim. En 2025, la production de Cerro Lindo a été de 87 000 t de Zn, 27 000 t de Cu, 10 000 t de Pb, 132,724 t de Ag et en 2024, 153 kg de Au et les réserves prouvées et probables sont de 39 millions de t renfermant 1,38 % de Zn, 0,52 % de Cu, 0,20 % de Pb, 21,4 g/t de Ag. La production de Vazante a été de 128 000 t de Zn, 900 t de Pb et 12 t de Ag et les réserves prouvées et probables sont de 13,75 millions de t renfermant 8,22 % de Zn, 0,25 % de Pb et 11,5 g/t de Ag.
- La mine à ciel ouvert de Wulagen, dans la province du Xinjiang, en Chine, est exploitée par le groupe chinois Zijin Mining avec, en 2024, une production de 140 803 t de Zn et 24 801 t de Pb.
- La deuxième plus importante mine européenne est celle de Tara en Irlande, exploitée par Boliden. En 2025, la mine a produit 76 000 t de Zn, 7 000 t de Pb et 642 kg de Ag. Les réserves prouvées et probables sont de 16,6 millions de t de minerai contenant 5,4 % de Zn et 1,3 % de Pb. En juillet 2023, l’exploitation minière a été suspendu et a repris en 2025.
- La mine souterraine de Neves Corvo, dans la province de l’Alentejo, au Portugal, était exploitée par Lundin Mining. Elle comporte deux zones, l’une riche en cuivre, l’autre riche en zinc. En 2025, la production est de 78 000 t de Zn, 23 000 t de Cu, 6 000 t de Pb et 42 kg de Ag. Les réserves prouvées et probables sont, pour la zone riche en cuivre de 23,9 millions de t renfermant 2,48 % de Cu, 0,6 % de Zn, 0,2 % de Pb et 31,6 g/t de Ag et pour le zone riche en zinc de 24,2 millions de t renfermant 0,32 % de Cu, 6,7 % de Zn, 1,5 % de Pb et 57 g/t de Ag. Courant 2022, la capacité de production en concentrés de zinc est passée de 75 000 à 155 000 t/an de zinc contenu et est devenue la plus importante mine européenne de zinc. En avril 2025, la mine a été acquise par Boliden sous l’appellation Somincor.
Minéralurgie ou concentration :
Après extraction du minerai, celui-ci subit un traitement physique consistant à éliminer une grande partie de la gangue. Dans le cas des minerais sulfurés, une flottation est généralement effectuée. Elle consiste à séparer d’une part les parties valorisables d’un minerai et d’autre part la gangue, en jouant sur leurs propriétés de surface et plus particulièrement sur le caractère hydrophobe ou hydrophile (mouillant) de celles-ci.
Avant de pouvoir séparer les constituants du minerai, il faut « libérer » les particules valorisables par broyage qui sera d’autant plus poussé que, par exemple les sulfures métalliques à récupérer, seront disséminés dans le minerai sous forme de fines particules. Ainsi, les blocs de quelques m3 extraits de la mine seront broyés jusqu’à atteindre quelques dizaines à quelques centaines de micromètres.
La flottation est réalisée dans des cuves dans lesquelles le minerai broyé est mis en suspension aqueuse. Des ajouts éventuels sont effectués pour ajuster le pH, modifier les propriétés de surface des particules à l’aide de collecteurs, former des mousses stables. D’autres ajouts permettent de moduler l’action des agents collecteurs : des déprimants augmentent le mouillage, des activateurs annihilent les effets des déprimants. Par ailleurs, une arrivée d’air permet de former des bulles qui entraînent en surface les éléments valorisables qui se retrouvent dans des mousses en formant une écume. Cette dernière, après séchage, donne des concentrés.
Il est également possible de séparer sélectivement divers sulfures métalliques d’une part de la gangue et d’autre part entre eux.
Après flottation les concentrés contiennent de 40 à 60 % de Zn (en moyenne 53 %) sous forme de sulfure de zinc ZnS. Lors de la flottation le zinc n’est pas transformé chimiquement, il reste sous forme de sulfure.
En général, la concentration est effectuée dans des installations voisines de l’extraction minière, les concentrés étant évacués, souvent par voie maritime, vers les installations de traitement métallurgique. Le schéma ci-dessous illustre les opérations de concentration par flottation.
Schéma de principe d’un circuit de flottation différentielle
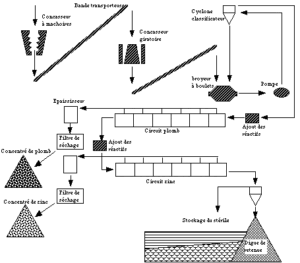
Exemple de flottation concernant un minerai contenant de la blende, de la pyrite et de la galène, dans une gangue de calcite et de dolomie.
Broyage : le minerai a été broyé pour que 80 % du produit passe au tamis de 170 microns.
Flottation : les résultats moyens du traitement par flottation sont les suivants :
| Produits | Masse en % | Teneur en Pb | Teneur en Zn |
| Tout-venant | 100,0 % | 5,7 % | 6,9 % |
| Concentré de galène | 7,2 % | 70,9 % | 3,6 % |
| Concentré de blende | 10,3 % | 0,5 % | 52,1 % |
| Rejet final | 82,5 % | 0,7 % | 1,6 % |
Consommations de réactifs :
| Circuit plomb | Circuit zinc | ||||
| CaO | 1500 g/t | CaO | 2560 g/t | ||
| NaCN | 70 g/t | CuSO4 | 300 g/t | ||
| Ethyl et amylxanthate | 70 g/t | Ethyl et amylxanthate | 120 g/t | ||
| Huile de pin | 5 g/t | ||||
Composition des concentrés obtenus :
| Éléments | Zn | S | Pb | Cu | Cd | Fe | Sn | Bi | CaO | MgO | SiO2 | Al2O3 | Ag | Sb | As |
| Concentré de galène | 4,7% | 16,7% | 70,0% | 1,0% | 6,0% | 0,02% | 0,6% | 0,4% | 800g/t | 0,2g/t | 0,3g/t | ||||
| Concentré de blende | 50,3% | 31,5% | 1,0% | 0,50% | 0,15% | 11,1% | 0,007% | 0,5% | 0,3% | 0,25% | 0,8% | 70g/t | 0,01g/t | 0,15g/t |
Productions minières
Production minière de zinc
En milliers de t de zinc contenu, en 2025, sur un total mondial de 13 millions de t. Source : USGS
| Chine | 4 100 | États-Unis | 670 | |
| Pérou | 1 500 | Bolivie | 500 | |
| Australie | 1 100 | Russie | 430 | |
| Inde | 870 | Kazakhstan | 360 | |
| Mexique | 780 | Suède | 230 |
Sources : ilzsg et USGS
En 2025, la production minière mondiale est de 12,586 millions de t.
La production de l’Union Européenne (Suède, Irlande, Portugal, Espagne, Pologne, Finlande…), en 2017, est de 683 400 t.
Commerce international : en 2024.
Principaux pays exportateurs sur un total mondial de 11,592 millions de t de concentrés.
| Pérou | 1 873 | Bolivie | 537 | |
| Australie | 1 867 | Belgique | 535 | |
| Mexique | 980 | Kazakhstan | 431 | |
| Turquie | 748 | Suède | 399 | |
| États-Unis | 665 | Chili | 399 |
Les exportations péruviennes sont destinées à la Chine à 46 %, à l’Espagne à 12 %, à la Corée du Sud à 10 %, au Brésil à 7 %.
Principaux pays importateurs, sur un total de 11,997 millions de t.
| Chine | 4 094 | Finlande | 578 | |
| Corée du Sud | 1 522 | Canada | 464 | |
| Belgique | 903 | Iran | 410 | |
| Espagne | 831 | Pays Bas | 348 | |
| Japon | 676 | Norvège | 283 |
Les importations chinoises proviennent d’Australie à 21 %, du Pérou à 18 %, du Kazakhstan à 7 %, d’Afrique du Sud à 6 %.
Principaux producteurs : en 2024
| Glencore (Suisse), en 2025 | 969 | Industrias Peñoles (Mexique) | 271 | |
| Hindustan Zinc (Inde), en 2024-25 | 863 | Trafigura (Suisse) | 250 | |
| Teck (Canada), en 2025 | 565 | Volcan (Pérou), en 2025 | 235 | |
| Zijin Mining (Chine) | 407 | MMG (Chine), en 2025 | 232 | |
| Nexa Resources (Brésil), en 2025 | 316 | Boliden (Suède), en 2025 | 351 |
Sources : Boliden et rapports des sociétés
- Glencore exploite, en 2025, des mines de zinc :
- en Australie, dans le Queensland, à Mount Isa et Lady Loretta avec une production de 288 200 t de zinc et Mc Arthur River avec 274 600 t,
- au Kazakhstan avec 212 500 t, la mine de Zhairem, est entrée en production, en 2021, avec une capacité prévue de 150 000 t/an,
- au Canada, à Kidd avec 41 500 t,
- au Pérou à Antamina avec 152 600 t.
- La Compañia Minera Volcan exploite, au Pérou, diverses unités minières, Yauli (4 mines souterraines) avec, en 2025, 162 000 t de Zn, 25 000 t de Pb, 3 000 t de Cu, 218 t de Ag, Chungar (2 mines souterraines) avec, 42 200 t de Zn, 21 200 t de Pb, 900 t de Cu, 53,5 t de Ag, Alpamarca (une mine souterraine et une à ciel ouvert) avec, 4 500 t de Zn, 3 500 t de Pb, 200 t de Cu, 22 t de Ag et Cerro de Pasco avec 26 400 t de Zn, 13 600 t de Pb, 25 t de Ag. En 2025 a produit un total de 235 500 t de Zn, 63 700 t de Pb, 3 900 t de Cu et 420 t de Ag. Fin 2025, les réserves prouvées et probables de Volcan sont de 47,2 millions de t renfermant 3,72 % de Zn, 1,24 % de Pb, 0,06 % de Cu et 62 g/t de Ag.
De fin 2017 à mai 2024 a été détenue à 23 % par Glencore qui a vendu sa participation à Transition Metals, filiale d’Integra Capital. - Vedanta exploite, en Inde, à Rampura-Agucha, dans le Rajasthan, l’une des plus importantes mines au monde, ainsi que 4 autres mines, toutes souterraines, Kayad, Sindesar, Rajpura et Zawar, au travers de Hindustan Zinc Limited (HZL), société possédée à 64,9 %, l’État indien en détenant 29,5 %, avec, en 2024-25 une production de 863 000 t de zinc, 232 000 t de plomb et 687 t d’argent. En mai 2010, Vedanta a acquis les activités d’Anglo American dans le zinc et le plomb, avec les mines de Skorpion en Namibie (fermée en 2020) et Black Mountain en Afrique du Sud (44 000 t de Zn et 39 373 t de Pb, en 2023-24), détenue à 74 %. En Afrique du Sud, développe le projet de la mine de Gamsberg avec une production de 133 000 t de Zn et 86 t de Pb, en 2023-24.
- Teck, a produit, en 2025, 565 000 t de zinc contenu dans des concentrés lors de l’exploitation des mines :
- de Red Dod, en Alaska, avec 462 700 t,
- Antamina, au Pérou avec une participation de 22,5 % d’une production de 454 000 t, soit 102 000 t.
- Zijin Mining exploite des mines de zinc en Chine, en Russie et en Érythrée. A produit, en 2024, 407 077 t de zinc, 44 397 t de plomb, 435,8 t d’argent et 72,9 t d’or.
- Les mines chinoise sont celles de Wulagen dans le Xinjiang, à ciel ouvert, avec 140 803 t de Zn et 24 801 t de Pb et de Miaogou en Mongolie Intérieure, souterraine, avec 53 354 t de Zn et 11 849 t de Pb, ainsi que la mine souterraine de cuivre de Habahe Ashele dans le Xinjiang, détenue à 51 %, avec 8 729 t de Zn et 22 441 t de Cu,
- en Russie détient 70 % de la mine de Kyzyl-Tash Turk, dans la République de Tuva, avec 71 272 t de Zn et 4 748 t de Pb,
- en Erythrée exploite la mine à ciel ouvert de Bisha avec 121 401 t de Zn et 65 t de Ag.
- Nexa Resources détenu à 64,25 % par Votorantim, exploite :
- au Pérou les mines de Cerro Lindo, avec, en 2025, une production de 87 000 t de zinc contenu, El Porvenir avec 53 000 t, Atacocha avec 12 000 t,
- au Brésil, dans l’État du Minas Gerais, les mines de Vazante avec 128 000 t et dans l’État de Mato Grosso, la mine d’Aripuaña avec 31 6135 000 t.
- Industrias Peñoles exploite, au Mexique, de nombreuses mines, avec, en 2024, une production de 270 847 t de zinc contenu. En 2024, dans l’État de Durango, la mine de Velardeña a produit 80 941 t, dans l’État de Zacatecas, celle de Sabinas 12 848 t, dans l’État de Mexico, celle de Tizapa, détenue à 51 %, 26 935 t, dans l’État de Guerrero celle de Capela 20 327 t. Par ailleurs Industrias Peñoles détient 74,99 % de la société Fresnillo qui exploite des métaux précieux, au Mexique, dans 8 mines dont 5 produisant du zinc, avec 116 646 t.
- Trafigura qui a repris les activités de Nyrstar exploite 5 mines souterraines de zinc aux États-Unis dans le Tennessee. La production a été suspendue dans 2 mines en novembre 2023.
- Boliden exploite :
- en Suède, les mines de Renstrom, Kristineberg, Kankberg et Mouliden qui ont produit, en 2025, 43 000 t de Zn, 3 000 t de Cu, 4 000 t de Pb, 48,4 t de Te, 72,9 t de Ag et 2,5 t de Au ainsi que les mines de Garpenberg avec 102 000 t de Zn, 700 t de Cu, 39 000 t de Pb, 256 t de Ag et 747 kg de Au,
- en Irlande, la mine de Tara avec 76 000 t de Zn, 7 000 t de Pb et 642 kg de Ag.
- au Portugal, la mine de Neves Corvo via la société Somincor, acquise en avril 2025, avec 78 000 t de Zn, 23 000 t de Cu, 6 000 t de Pb et 42 kg de Ag.
- en Suède, la mine de Zinkgruvan, acquise en avril 2025, avec 52 000 t de Zn, 3 000 t de Cu, 21 000 t de Pb et 54 kg de Ag.
- MMG, détenu par le groupe chinois China Minmetals, exploite, en Australie, la mine de Dugald River, dans la province du Queensland, avec, en 2025, une production de 183 463 t de Zn et celle de Rosebery, en Tasmanie, avec 48 597 t de Zn.
- La production de Sumitomo Corporation, société japonaise, provenait principalement de la mine de San Cristobal, en Bolivie, vendue, en 2023. Par ailleurs Sumitomo détient une participation de 10 % dans la mine de Tizapa, au Mexique.
Réserves minières de zinc
En millions de t zinc contenu, en 2025, sur un total mondial de 240 millions de t. Source : USGS
| Australie | 64 000 | Inde | 10 000 | |
| Chine | 60 000 | États-Unis | 9 300 | |
| Russie | 29 000 | Kazakhstan | 7 400 | |
| Pérou | 18 000 | Bolivie, en 2022 | 4 800 | |
| Mexique | 14 000 |
Situation française : en 2025.
Production : Les mines, exploitées par Metaleurop, ont fermé en décembre 1991 pour les Malines (30) et en décembre 1993 pour St Salvy (81).
Commerce extérieur :
Les exportations étaient de 49 805 t avec comme principaux marchés à :
- 30 % la Norvège,
- 28 % les Pays Bas,
- 23 % la Belgique,
- 18 % la Finlande.
Les importations s’élevaient à 285 747 t en provenance principalement à :
- 24 % du Mexique,
- 15 % de Bolivie,
- 14 % d’Allemagne,
- 8 % du Canada,
- 7 % de Finlande.
Métallurgie de première fusion
Elle s’effectue en 2 étapes : un grillage est suivi par une réduction.
Grillage
Il est réalisé par chauffage, à 900 – 1100°C, en présence d’air, selon la réaction :
ZnS + 3/2 O2 = ZnO + SO2 Δr H°298 = – 460 kJ/mole.
Des réactions parasites sont susceptibles de se produire, principalement, la formation de sulfate selon des réactions qui ont lieu à 500-600°C, le sulfate formé étant décomposé vers 900°C :
ZnO + SO2 + 1/2 O2 = ZnSO4
ZnS + 2 O2 = ZnSO4
Lorsque le concentré est riche en fer, ce qui est souvent le cas, il se forme des ferrites, oxydes mixtes de zinc et de fer, selon la réaction :
ZnO + 2 FeS + 7/2 O2 = ZnFe2O4 + 2 SO2
Ces ferrites sont insolubles dans l’acide sulfurique dilué utilisé lors des opérations hydrométallurgiques et leur présence a longtemps été un obstacle à ces opérations.
Les autres éléments métalliques qui accompagnent le zinc dans le concentré minier subissent le même type de transformation : les sulfures sont transformés en oxydes.
Le dioxyde de soufre formé, avec une teneur de 6 à 7 % dans le gaz évacué du grillage, est récupéré et transformé en acide sulfurique (jusqu’à 2 t de H2SO4/t de Zn). Ainsi, les producteurs de zinc, ainsi que ceux de plomb, sont également producteurs d’acide sulfurique. A l’usine d’Auby, en France, 99,5 % du SO2 produit lors du grillage est transformé en H2SO4 selon le procédé de contact à double catalyse, la production a été, en 2018, de 167 000 t d’acide pour une production de 155 000 t de zinc.
Le concentré de zinc, après grillage, est appelé calcine.
La réalisation industrielle du grillage dépend des procédés métallurgiques de réduction utilisés par la suite.
- Si la réduction est effectuée par hydrométallurgie, il faut que la finesse initiale du concentré soit préservée afin de faciliter l’attaque acide. Il faut donc éviter tout frittage de la calcine et opérer plutôt à basse température (900-950°C). La présence de sulfate, en faible teneur, n’est pas gênante.
Dans ce cas, un grillage en lit fluidisé est utilisé : les particules à griller sont mises en suspension dans de l’air qui est insufflé à travers des orifices, de 5 mm de diamètre, présents dans la sole du four. Le débit d’air est d’environ 10 m3/min/m2 de sole. La combustion a lieu vers 900-950°C. La teneur résiduelle en soufre, principalement sous forme de sulfate, est de 1,5 à 2 %. En France, lors du grillage de ses concentrés de zinc, l’usine Nyrstar d’Auby (59) utilise ce procédé (procédé Vieille Montagne – Lurgi qui est le plus répandu dans le Monde). Le four de grillage de Nyrstar à Balen, en Belgique, grille 850 t de concentrés/jour. - Si la réduction est effectuée par pyrométallurgie (qui concerne les concentrés riches en plomb), selon des techniques proches de celles du haut fourneau, il faut que la calcine puisse supporter la charge du four et donc posséder une bonne résistance mécanique à l’écrasement tout en restant poreuse pour que le monoxyde de carbone puisse la réduire. La calcine est agglomérée par frittage lors d’un grillage effectué à haute température (1000°C et plus). La teneur en soufre total (sous forme de sulfure et de sulfate) doit être la plus faible possible (< 0,5 %).
Dans ce cas, un grillage sur machines Dwight et Lloyd est utilisé : ce type de grillage est également utilisé pour les concentrés de plomb qui sont, en général, réduits par pyrométallurgie. Les machines Dwight et Lloyd se présentent comme une bande sans fin de chariots mobiles munis de grilles, glissant sur des caissons étanches. L’air est soufflé à travers les grilles. La température de grillage est d’environ 1000°C (voir le chapitre consacré au plomb). La réaction de grillage étant très exothermique, afin d’éviter des températures trop élevées qui en faisant fondre le sulfure de plomb diminueraient la porosité de la charge, le concentré cru est dilué dans de la calcine déjà formée à des taux de 12 à 20 %.
Diaporama sur : le grillage des concentrés de zinc
Réduction
Elle est effectuée selon 2 procédés :
- Hydrométallurgique qui concerne 90 % de la production.
- Pyrométallurgique (ou procédé thermique).
Hydrométallurgie
Elle se déroule en 4 étapes.
Lixiviation : la calcine est attaquée par une solution diluée d’acide sulfurique (180 à 190 g/L). Cette solution est récupérée, à la fin de l’électrolyse, pour être recyclée en amont des opérations hydrométallurgiques. Elle contient également de 30 à 50 g/L d’ions Zn2+ qui n’ont pas été récupérés totalement par électrolyse et qui sont ainsi recyclés. La dissolution est effectuée vers 55 à 65°C, la chaleur étant apportée par la dissolution des oxydes. L’oxyde de zinc passe en solution selon la réaction représentée par l’équation chimique suivante :
ZnO + 2 H+ + SO42- = Zn2+ + SO42- + H2O
Les autres oxydes métalliques présents dans la calcine passent également en solution sauf l’oxyde de plomb qui donne du sulfate de plomb très peu soluble. Les métaux précieux, argent et or, restent insolubles ainsi que, en général, la gangue, si celle-ci est siliceuse.
La dissolution de ZnO et des autres oxydes se traduit par une consommation d’acide et donc par une augmentation de pH. Cette dissolution dure de 1 à 4 heures et de 75 à 90 % du zinc passe en solution. Le zinc qui reste insoluble est celui qui, lors du grillage, a formé, avec l’oxyde ferrique, des ferrites. Ce zinc est récupéré par une opération complémentaire.
Élimination des ions ferriques : lors de la lixiviation, appelée lixiviation neutre, le milieu est rendu oxydant par injection d’air ou de dioxygène ou par ajout de dioxyde de manganèse ou de permanganate de potassium afin, principalement, d’oxyder les ions Fe2+, éventuellement présents, en ions Fe3+. A ce stade, tous les ions Fe3+ ne sont pas dissous, une partie est incluse dans les ferrites insolubles. La solution passe, de façon continue, de cuves en cuves, le pH de la solution augmentant progressivement, par ajout de calcine, pour atteindre 5 dans la dernière cuve. A ce pH, l’hydroxyde ferrique précipite. Une décantation permet de séparer la solution des résidus insolubles.
Le résidu solide peut contenir, si le minerai de départ est riche en fer, une part importante du zinc initialement présent dans le minerai. Il est nécessaire de récupérer ce zinc en attaquant ce résidu, à chaud, vers 90-95°C, par la solution d’acide sulfurique provenant de l’électrolyse. Dans ces conditions, la ferrite est dissoute et les ions contenus, Fe3+ et Zn2+, passent en solution. Cette opération est appelée lixiviation acide.
Toute la difficulté de l’hydrométallurgie du zinc réside, pour les minerais riches en fer, ce qui est le cas de ceux actuellement exploités, dans l’élimination des ions ferriques. En effet, par élévation de pH, l’hydroxyde ferrique Fe(OH)3 précipite. Celui-ci peut être séparé d’une solution par décantation : c’est ce qui se produit lors de la « lixiviation neutre ». Mais, si on souhaite, et cela est le cas industriellement, récupérer au maximum les ions Zn2+ de la solution, il est nécessaire de filtrer et de laver le précipité. Or, l’hydroxyde ferrique est très difficile, sinon impossible industriellement, à filtrer. Pour résoudre cette difficulté, plusieurs procédés sont utilisés, le plus employé a été longtemps celui dit « à la jarosite », les jarosites formant une famille de composés de formule Fe6(OH)12(SO4)4M2 avec M = Na+, K+, NH4+, Ag+, H3O+… Le procédé le plus employé actuellement est celui dit « à la goethite ». La solution provenant de la lixiviation acide est traitée, à 95°C, par de la blende non grillée. Les ions Fe3+ sont réduits en Fe2+ selon la réaction :
2 Fe3+ + ZnS = 2 Fe2+ + Zn2+ + S
Le résidu solide, contenant le soufre formé et la blende non dissoute, réintègre le circuit de traitement en amont du grillage.
Le pH de la solution est augmenté, par ajout de calcine, pour atteindre environ 3, en présence de dioxygène pur ou d’air afin d’oxyder les ions Fe2+. La réaction mise en jeu est la suivante :
4 Fe2+ + 4 ZnO + O2 + 2 H2O = 4 FeO(OH) + 4 Zn2+
Les ions Fe3+ précipitent sous forme de goethite FeO(OH) et sont ainsi éliminés de la solution qui contient moins de 1 g/L d’ions Fe3+.
La solution issue de la lixiviation acide réintègre le circuit de traitement, en amont de la « lixiviation neutre ». En même temps que les ions ferriques, les éléments suivants sont éliminés par précipitation : Al, Ga, In, Sb, Sn, As et Ge.
Purification de la solution : après lixiviation, dans la solution, outre Zn2+, les ions suivants sont encore présents : Cu2+, Cd2+, Ni2+, Co2+, Mn2+. L’élimination de la plupart d’entre eux est effectuée par réduction à l’aide de poudre de zinc. L’emploi de zinc permet d’éviter l’introduction d’ions étrangers. Les ions Mn2+, non réduits, resteront en solution, mais par contre, les autres ions seront réduits selon la réaction, avec M = Cu, Cd, Ni, Co :
Zn + M2+ = Zn2+ + M
Les ions Cu2+ et Cd2+ sont très facilement réduits, cela est plus difficile pour Ni2+ et Co2+ qui demandent la présence d’activateurs et une température de 75 à 95°C. Ces métaux se déposent sur les particules de zinc, d’environ 30 micromètres de diamètre, en excès. La quantité de zinc utilisée dépend de la teneur en impuretés, elle varie de 16 à plus de 100 kg/t de zinc produit. Cette opération de purification, appelée cémentation, est réalisée, en continu, durant plusieurs heures (de 1 à 8 h). Une filtration sur toile très fine permet de récupérer les particules de zinc enrobées par les métaux déposés. Ce solide, appelé cément, est traité afin de récupérer les métaux contenus et en particulier le zinc.
La teneur finale de la solution est, en général, pour chacun des ions Cu2+, Cd2+, Ni2+ et Co2+ inférieure à 0,5 mg/L. La solution de Zn2+, est ainsi purifiée des ions susceptibles de se déposer, par électrolyse, en même temps que Zn.
Électrolyse : elle est réalisée, dans des cuves en ciment revêtue de PVC, vers 30 à 40°C. La solution contient initialement de 125 à 170 g/L de Zn2+.
Les anodes sont en alliage de plomb contenant de 0,5 à 1 % de Ag inattaquable en milieu sulfate, les cathodes sont en aluminium. L’intérêt de l’emploi de cathodes en aluminium réside dans le fait que celles-ci, au pH utilisé – vers 5, sont recouvertes par une couche d’alumine qui évite le contact direct du zinc déposé avec l’aluminium et ainsi la formation à l’interface d’un alliage qui empêcherait la récupération facile du zinc sans détérioration de la cathode.
La tension est comprise entre 3,2 et 3,7 V, avec une densité de courant de 400 à 700 A/m2. L’intensité atteint jusqu’à 115 000 A.
Le zinc se dépose sur la cathode d’où il est décollé toutes les 24, 48 ou 72 heures par pelage (ou stripping). La production, par cellules qui contiennent jusqu’à 86 cathodes de 1,6 m2, peut atteindre 3 t/jour. La consommation d’énergie est de 3 000 à 3 500 kWh/t de Zn produit. Le zinc obtenu très pur (99,995 %) contient moins de 50 ppm d’impuretés, la principale étant le plomb. Il n’a pas besoin de subir un raffinage ultérieur. Les ions Mn2+ qui restent dans la solution s’oxydent en MnO2 sur l’anode en plomb.
La solution, après épuisement partiel (au 2/3) des ions Zn2+ et régénération de l’acide à l’anode, avec dégagement de dioxygène, est recyclée en amont des lixiviations neutre et acide.
Diaporama sur : l’hydrométallurgie du zinc
Pyrométallurgie
Concerne les minerais riches en plomb et en autres impuretés métalliques valorisables. La réduction a lieu dans des fours horizontaux ou verticaux par réduction avec le carbone ou selon le procédé Imperial Smelting par réduction avec le dioxyde de carbone (voir le chapitre consacré au plomb). Un raffinage du zinc d’œuvre (à 98,5 %) ainsi obtenu est nécessaire. La difficulté principale de la pyrométallurgie du zinc réside dans la température d’ébullition du zinc, 907°C, inférieure aux températures de réduction possibles thermodynamiquement avec le carbone ou le monoxyde de carbone. Le zinc, à l’état gazeux, peut ainsi être rapidement réoxydé par le monoxyde ou le dioxyde de carbone formé lors de son refroidissement. En conséquence, la vapeur doit être refroidie le plus rapidement possible (voir les diagrammes d’Ellingham dans le diaporama ci-dessous). La réduction par le carbone est cinétiquement facilitée par la formation de zinc gazeux mais le chauffage du four doit être réalisé par l’extérieur de ce dernier afin d’éviter que les produits de la combustion, en particulier le dioxyde de carbone, réoxydent le zinc.
Le raffinage est réalisé par distillations fractionnées selon le procédé New Jersey. Le plomb est éliminé dans une première colonne, puis le cadmium dans une seconde (température d’ébullition de Cd : 767°C). On obtient du zinc à 99,99 % qui est coulé en lingots de 25 kg.
Diaporama sur : la pyrométallurgie du zinc
Productions métallurgiques
Production métallurgique (primaire et secondaire) de zinc
En milliers de t, en 2025, sur un total de 13,830 millions de t. Source : ilzsg
| Chine | 7 000 | Australie | 448 | |
| Inde | 864 | Japon | 390 | |
| Corée du Sud | 774 | Mexique, en 2021 | 357 | |
| Espagne, en 2023 | 504 | Pérou | 348 | |
| Canada | 532 | Kazakhstan | 260 |
Source : ilzsg
En 2025, la production mondiale est de 13,830 millions de t.
La production de l’Union européenne est, en 2020, de 1,515 million de t.
Commerce international du zinc brut : en 2024.
Exportations sur un total de 5,173 millions de t, en 2023 :
| Belgique | 510 | Pérou | 280 | |
| Corée du Sud | 460 | Finlande | 253 | |
| Pays Bas | 411 | Kazakhstan | 247 | |
| Australie | 404 | Inde | 222 | |
| Canada | 381 | Mexique | 206 |
Source : ITC
Les exportations belges sont destinées à l’Allemagne pour 18 %, l’Italie pour 14 %, les Pays Bas pour 13 %, la France pour 10 %, la Turquie pour 6 %.
Importations :
| États-Unis | 595 | Vietnam | 267 | |
| Chine | 495 | Belgique | 242 | |
| Allemagne | 367 | Italie | 219 | |
| Pays Bas | 343 | Singapour | 214 | |
| Turquie | 299 | Inde | 200 |
Source : ITC
Les importations des États-Unis proviennent à 62 % du Canada, 17 % du Mexique, 11 % du Pérou, 5 % du Brésil.
Principaux producteurs mondiaux : en 2024.
| Glencore (Suisse) | 1 060 | Hechi Nanfang (Chine) | 500 | |
| Korea Zinc Group (Corée du Sud) | 1 020 | Boliden (Suède), en 2025 | 457 | |
| Trafigura (Suisse) | 860 | Shaanxi Non ferrous Metals (Chine) | 310 | |
| Hindustan Zinc (Inde), en 2024-25 | 827 | Zijin Mining (Chine) | 300 | |
| Nexa Resources (Brésil), en 2025 | 532 | Teck Resources (Canada), en 2025 | 230 |
- Korea Zinc Group, produit :
- en Corée du Sud, à Onsan, avec, en 2021, des ventes de 636 799 t de Zn, 429 022 t de Pb, 27 443 t de Cu, 2 226 t de Ag et 13,9 t de Au et à Sukpo, avec 400 000 t/an de Zn par sa filiale Young Poong,
- en Australie, par sa filiale Sun Metals Company, à Townville, dans le Nord Queensland, avec, en 2021, une production de 206 780 t de Zn.
- En 2018, la production de Nyrstar depuis devenu filiale de Trafigura, groupe de négoce, a été de 1,064 million de t de zinc, 1,364 million de t d’acide sulfurique, 160 000 t de plomb, 4 300 t de cuivre, 42,6 t d’indium, 423 t d’argent, 2,27 t d’or. La production de zinc est réalisée dans les usines :
- de Balen/Overpelt (Belgique) avec 285 000 t/an,
- Hobart (Australie) avec 265 000 t/an,
- Budel (Pays-Bas) avec 293 000 t/an,
- Clarksville (Tennessee, États-Unis) avec 101 000 t/an,
- Auby (France) avec 172 000 t/an.
- Par ailleurs, Nyrstar possède des participations dans des usines chinoises, en particulier à Kunming (Yunnan).
- En 2024-25, la production de Hindustan Zinc, en Inde, a été de 827 000 t de Zn, 225 000 t de Pb et 687 t de Ag. Les fonderies sont situées au Rajasthan, à Chanderiya avec une production, en 2021-22 de 585 000 t de Zn et 90 000 t de Pb, Debari avec 88 000 t de Zn et Dariba avec 240 000 t de Zn et 120 000 t de Pb.
- En 2024, Glencore a produit :
- au Kazakhstan, à Ust Kamenogorsk et Ridder, 128 300 t de zinc, avec sa filiale Kazzinc,
- en Italie, en Sardaigne, à Portovesme, avec une capacité de 150 000 t/an,
- en Espagne, à San Juan de Nieva, par la société Asturiana de Zinc, avec 510 510 t, en 2020,
- en Allemagne, à Nordenham, avec 175 000 t/an,
- en Argentine, à Santa Fé, avec 26 100 t de zinc,
- au Canada, province du Québec, à Salaberry-de-Valleyfield, avec la raffinerie CEZ (Canadian Electrolytic Zinc) et une part de 25 % d’une production, en 2021, de 264 046 t.
- Nexa Resources, produit du zinc au Pérou, dans sa raffinerie de Cajamarquilla avec, en 2025, 346 000 t de Zn, ainsi qu’au Brésil, à Três Marias avec 122 000 t de Zn et 35 000 t d’oxyde de zinc et à Juiz de Fora avec 64 000 t de Zn.
- En 2025, Boliden, en Suède, a produit 457 000 t de zinc dans ses raffineries de Kokkola avec 290 000 t de Zn et 312 000 t d’acide sulfurique et de Odda, avec 167 000 t de Zn et 124 000 t d’acide sulfurique.
- Teck Resources, produit du zinc dans sa raffinerie de Trail en Colombie Britannique, au Canada. En 2025, la production est de 229 900 t de Zn, 80 100 t de Pb et 355 t de Ag.
- Le groupe russe Chelyabinsk possède une capacité de production de 215 000 /an. En 2020, la production est de 211 781 t de Zn.
Principales usines :
| Onsan (Korea Zinc), Corée du Sud | 645 | Sukpo (Korea Zinc), Corée du Sud | 400 | |
| Chanderiya (Hindustan Zinc), Inde | 558 | Cajamarquilla (Nexa Resources), Pérou | 342 | |
| San Juan de Nieva (Glencore), Espagne | 504 | Mian Xian (Shaanxi Non ferrous Metals), Chine | 340 | |
| Zhuzhou (Minmetals), Chine, Hunan | 420 | Trail (Teck), Canada | 310 |
L’usine de Chanderiya, exploitée par Hindustan Zinc, possède une capacité de production de 480 000 t/an par hydrométallurgie et 105 000 t/an par pyrométallurgie. En 2019-20, la production a été de 425 780 t de zinc et 94 916 t de plomb.
L’usine de San Juan de Nieva, en Espagne, exploitée par l’Asturiana de Zinc, propriété du groupe Glencore, est l’usine de production de zinc la plus importante en Europe avec, en 2022, 504 011 t.
Recyclage
Métallurgie de seconde fusion (affinage) : le zinc obtenu est appelé secondaire.
Le zinc récupéré après usage ainsi que les chutes et déchets des usines métallurgiques sont soit réutilisés directement, soit réemployés après refusion (c’est le cas, par exemple, des alliages de fonderie) soit encore retraités en suivant le circuit de la métallurgie de 1ère fusion (c’est le cas, en particulier, des oxydes de zinc).
Le zinc recyclé représente 45 % de la consommation mondiale. En 2020, aux États-Unis, la production de zinc secondaire est de 70 000 t, à côté d’une production primaire de 110 000 t. Dans ce pays, en 2022, le recyclage représente 60 % de la production. En Europe de l’ouest, le zinc utilisé comme couverture de toitures et pour recueillir les eaux pluviales est recyclé à 90 % ce qui représente 110 230 t/an.
Le zinc contenu dans les laitons (600 000 t de Zn/an) est recyclé par l’industrie du cuivre.
Le zinc de galvanisation se retrouve dans les ferrailles recyclées par la sidérurgie et peut être récupéré par traitement des poussières des aciéries électriques dans lesquelles Zn est sous forme de ZnO. 1 t d’acier produit 20 kg de poussières contenant de 15 à 30 % de Zn.
L’usine Recytech, détenue à 50 % par Recylex, à Fouquières-lez-Lens (62) traite, dans un four tournant selon le procédé Waelz, des poussières d’aciéries électriques, de fonderies et d’autres résidus zincifères pour récupérer, principalement de l’oxyde brut, appelé oxyde Waelz, contenant de 50 à 60 % de ZnO. La réduction est effectuée à l’aide de carbone, vers 1200°C. Le zinc se volatilise puis se réoxyde lors de son refroidissement. Cet oxyde est destiné à alimenter les usines de production de zinc raffiné. Recylex recycle également des poussières d’aciéries électriques et des déchets zincifères à Goslar-Oker, en Allemagne. Le groupe, en 2020, a produit 43 000 t d’oxydes Waelz à partir de poussières d’aciéries électriques.
L’économie circulaire du zinc, en 2018, en millions de t. Schéma simplifié d’après A. Green, « Overview of key initiative for zinc« , IZA (les variations des stocks ne sont pas prises en compte).
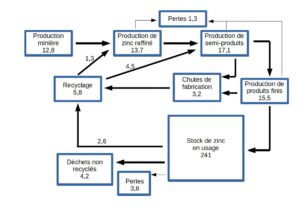
Situation française
Productions :
- Zinc primaire raffiné, en 2021 : 168 000 t.
- Zinc recyclé, en 2007 : 75 000 t.
Commerce extérieur : en 2025.
Exportations :
- Zn brut à teneur ≥ 99,99 % : 75 729 t vers la Belgique à 68 %, les Pays Bas à 29 %.
- Déchets : 64 913 t vers l’Italie à 34 %, la Belgique à 28 %, les Pays Bas à 18 %, la Thaïlande à 8 %.
- Poussières : 578 t vers la Belgique à 83 %, l’Italie à 11 %, la Pologne à 2 %.
Importations :
- Zn brut à teneur ≥ 99,99 % : 52 395 t des Pays Bas à 31 %, d’Espagne à 13 %, de Belgique à 12 %, de Finlande à 8 %, d’Allemagne à 7 %.
- Déchets : 45 068 t à 89 % d’Espagne, 5 % d’Italie.
- Poussière : 8 147 t de Belgique à 85 %, des Pays Bas à 13 %.
Usines :
Hydrométallurgie et grillage à Auby (59) par le groupe Nyrstar. En 2018, la production a été de 155 000 t de zinc, de 42,6 t d’indium et de 167 000 t d’acide sulfurique.
Recyclage avec Recytech (détenu 50/50 par Befesa Steel Service et Recylex) à Fouquières-lez-Lens (62) qui recycle les poussières d’aciéries électriques, de fonderies et d’autres résidus zincifères. En 2020, le traitement de 120 000 t de poussières et résidus de zinc a donné 43 000 t d’oxyde brut (oxyde Waelz).
Utilisations
Consommations mondiales : Monde, en 2025 : 13,863 millions de t, Union européenne, en 2014 : 2,361 millions de t.
| Chine | 7 050 | Japon | 328 | |
| États-Unis | 861 | Allemagne, en 2023 | 344 | |
| Inde | 855 | Italie, en 2023 | 267 | |
| Corée du Sud | 474 | Turquie, en 2023 | 266 | |
| Belgique, en 2023 | 380 | Mexique, en 2023 | 250 |
La consommation mondiale était de 3 millions de t en 1959 et de 10,57 millions de t, en 2005.
Formes d’utilisation du zinc
En 2023, dans le monde. Source ILZSG
| Monde, en 2023 | États Unis en 2020 | France, en 2007 | |
| Galvanisation | 60 % | 88,2 % | 49 % |
| Laiton et bronzes | 9 % | 7,5 % | 11 % |
| Autres alliages (Zamak…) | 15 % | 3,7 % | – |
| Demi produits | 4 % | 0,6 % | 35 % |
| Usages chimiques | 11 % | 4 % | |
| Autres produits | 1 % | 1 % |
En Chine, en 2017, la galvanisation représente 60 % des utilisations, les alliages autres que le laiton, 15 %, l’oxyde de zinc, 12 %, le laiton, 9 %, les batteries, 3 %.
En France, la production de demi-produits représente une part importante de la production, liée à l’utilisation importante des feuilles de zinc dans le bâtiment.
Secteurs d’utilisation : en 2023, dans le monde.
| Construction | 50 % | Équipements industriels | 7 % | |
| Transports | 20 % | Produits de consommation | 6 % | |
| Infrastructures | 15 % |
Source : ILZSG
Principales utilisations :
Revêtements anticorrosion dans l’acier zingué, voir ce chapitre. On estime que 10 % de la production mondiale d’acier est zinguée (80 % galvanisée, 20 % électrozinguée).
- Bâtiment : outre les utilisations dans l’acier galvanisé (avec parfois des revêtements à l’aide des alliages 55 % Al, 43,5 % Zn, 1,5 % Si ou 95 % Zn, 5 % Al, utilisés pour les toitures de bâtiments industriels), le zinc est utilisé pur ou faiblement allié. Le zinc est protégé de la corrosion par une couche passive de carbonate-hydroxyde de zinc (2ZnCO3,3Zn(OH)2). La vitesse moyenne annuelle de corrosion est de 1 micromètre en atmosphère rurale et de 10 micromètres en atmosphère industrielle. L’épaisseur moyenne du zinc laminé est de 0,7 mm. Des ajouts de Cu (0,1 % minimum) et Ti (0,05 % minimum) permettent de diminuer le coefficient de dilatation du zinc. Paris couvre ses toits, depuis le baron Haussmann, de zinc laminé : 5 millions de m2 de surface.
- Laitons : alliages avec Cu : 5 à 40 % de Zn (voir le chapitre alliages de cuivre). Le cuivre contenu dans le laiton confère à celui-ci un pouvoir bactéricide.
- Fonderie : les alliages « Zamak » (ZA4G, ZA4U1G, ZA4U3G) contenant de 3,9 à 4,3 % de Al, ainsi que Cu jusqu’à 3,5 % et Mg jusqu’à 0,06 % représentent 90 % de la production d’alliages de zinc de fonderie. Autres alliages de fonderie : ZA 8, ZA 27, Ilzro 12, Kayem. Dans les automobiles les pompes à essence sont en Ilzro. Dans un véhicule automobile moyen, de type européen, entre 10,2 kg de zinc dont 4,9 kg d’alliages, 3,2 kg dans le zingage des tôles et 0,5 kg dans les pneus.
Autres applications :
- Anodes sacrificielles : 450 t/an en France pour protéger les coques de navires, les citernes enterrées…
- Poussière de zinc : pour la fabrication de l’aniline, la stabilisation de matières plastiques, la cémentation de métaux précieux, la purification ultime des solutions d’électrolyse (voir le paragraphe hydrométallurgie), comme agent réducteur dans la fabrication des hydrosulfites de sodium et de la formaldéhyde, comme revêtement protecteur de l’acier dans les procédés dits de matoplastie et de shérardisation.
- Sel, poudre et zinc laminé : pour les anodes des piles salines et alcalines. Dans ces piles, le pôle positif est relié à un mélange de dioxyde de manganèse et de carbone (voir le chapitre consacré au manganèse). Les solutions d’électrolyte sont gélifiées (par de l’amidon) afin d’obtenir des piles sèches. Le pôle négatif est en zinc dont l’état dépend du type de pile.
Dans le cas des piles salines cylindriques, dans lesquelles l’électrolyte est soit du chlorure de zinc pur soit une solution fortement concentrée de ZnCl2 et de NH4Cl, le pôle négatif est constitué par un alliage de zinc (avec ajouts de Pb : 0,2 %) sous forme de godet. Le pôle positif est axial.
Dans le cas des piles alcalines, dans lesquelles l’électrolyte est KOH, le pôle négatif, axial, est constitué par un crayon de zinc entouré d’un aggloméré de poudre de zinc et est en contact avec la partie inférieure de la pile. Le boîtier, en acier, constitue le pôle positif. - Au début des années 80, aux États-Unis, les pièces de 1 cent qui étaient traditionnellement en cuivre ont été remplacées, par soucis d’économies, par des pièces de zinc recouvertes de Cu. La consommation de ces pièces est particulièrement importante, plusieurs milliers de t/an, du fait de la tradition de jeter ces pièces dans les fontaines.
- Agriculture : on estime que la moitié des sols agricoles ont un déficit en zinc. En 2015, la consommation mondiale de zinc est de 255 000 t dont 160 000 t en fertilisation, le reste dans l’alimentation animale. Dans ce secteur le sulfate de zinc représente 66 % de la consommation (77 % en fertilisation, 23 % en alimentation animale), l’oxyde de zinc représentant 34 % de la consommation (40 % en fertilisation, 60 % en alimentation animale). Les consommations en fertilisation en 2015, sont les suivantes :
| Inde | 60 000 t | Europe | 12 500 t | |
| Chine | 52 400 t | Australie | 12 400 t | |
| Reste de l’Asie | 49 500 t | Afrique | 10 000 t | |
| Amérique du Nord | 41 700 t | Europe de l’est et Asie centrale | 3 000 t | |
| Amérique latine | 15 600 t |
Source : IZA
- Organisme humain : les besoins sont de 12 à 15 mg/j nécessaires à l’activité de plus de 300 enzymes. L’organisme d’un homme de 70 kg contient de 2 à 3 g de zinc. Sa déficience entraîne en particulier, le nanisme… 1/3 de la population mondiale est affectée par un déficit en zinc ce qui entraîne 800 000 morts/an dans le monde.
Oxyde de zinc : préparé, par oxydation de produits de récupération et de déchets de zinc après vaporisation du zinc (procédé français) ou par réduction de concentrés miniers et combustion du zinc formé (procédé américain) ou encore par précipitation puis calcination à partir de solutions. Il entre dans la fabrication des caoutchoucs et pneumatiques car il accélère la vulcanisation, dans l’agriculture et l’alimentation animale (oligo-élément), en pharmacie (élément cicatrisant, crèmes pour protection UV), dans les varistances, les émaux et céramiques, les parafoudres moyenne tension du réseau électrique de l’EDF. En 2015, la production mondiale est de 1,6 million de t.
Umicore est un producteur important, avec 70 000 t/an, en Belgique, à Zolder, aux Pays Bas, à Eijsden, en Norvège, à Larvik, en Inde, à Goa.
Secteurs d’utilisation de ZnO : dans le monde, en 2015.
| Pneumatiques et caoutchoucs | 56 % | Agriculture | 7 % | |
| Céramiques et verres | 19 % | Peintures | 3 % | |
| Produits chimiques | 8 % |
Source : IZA
Diaporama sur : les utilisations du zinc
Bibliographie
- A3M, 17 rue de l’Amiral Hamelin, 75783 Paris Cedex 16.
- Économie et Géographie n°256, le zinc, juin-juillet 1988.
- Le gisement de Zinc de Noailhac-St Salvy, diapositives, CRDP Toulouse, 1985.
- HAU Jean-Marie, « Métallurgie du zinc », Techniques de l’Ingénieur », 2010.
- VIGNES Jean-Louis, ABDRABAH Manef, BABY Jean-Michel, « Une vie de zinc – Expériences sur l’élaboration, les propriétés et le recyclage d’un métal – les minerais et leur grillage« , BUP, n°766, juillet-août-sept. 1994.
- VIGNES Jean-Louis, ABDRABAH Manef, BABY Jean-Michel, EUSEBE C., « Une vie de zinc : l’hydrométallurgie« , BUP n°770, janvier 1995.
- VIGNES Jean-Louis et al, « Une vie de zinc : ses propriétés et son recyclage« , BUP n°790-91, janvier-février 1997.
- VIGNES Jean-Louis, ABDRABAH Manef, PIESSEN Philippe, BABBIT Michel, « Une vie d’acier zingué« , BUP n°790-91, janvier-février 1997.
- VIGNES Jean-Louis, JEHANNE Yves, « L’hydrométallurgie« , BUP n°857 (1), octobre 2003.
- The International Lead and Zinc Study Group, rua Almirante Barroso 38, 5th Floor, Lisbonne, 1000 – 013, Portugal.
- The International Zinc Association, 168 Avenue de Tervuren/Box4, B-1150 Bruxelles, Belgique.
- « Le zinc : revue de l’offre mondiale en 2021« , BRGM, juillet 2022.
- Zinc Oxide Producers Association (ZOPA).
- A. Kolodziejczak-Radjimska et T. Jesionowski, Zinc oxide – From synthesis to application : a review, Materials 2014, 7, 2833-81.
- Jean-Louis Vignes, « Du minerai au matériau », Paris de Sciences : 55èmes journées nationales de l’UdPPC – 26-29/10/2007.
Archives